

走进不朽情缘MG
NEWS不朽情缘MG的EcoliHCP检测优势
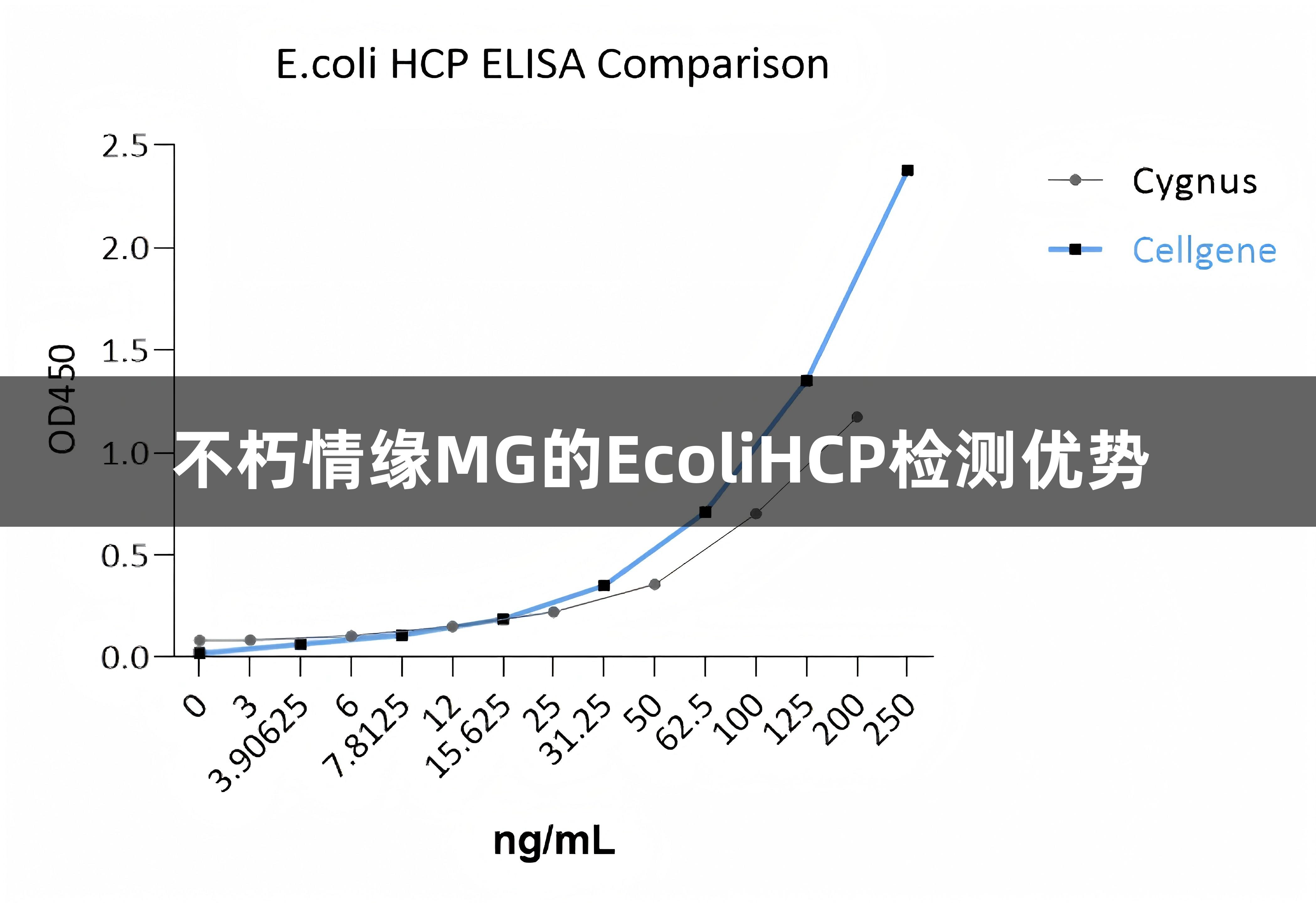
来源:温馨克 日期:2025-07-25不朽情缘MG在生物制药领域中,E. coli HCP(宿主细胞蛋白)产品性能的对比分析
在生物药物生产的发展历程中,针对药物最终产品中HCP杂质的有效去除与检测已有大量的研究和探索。这些杂质不仅对患者的安全构成威胁,还严重影响药物的稳定性。
目前,最常用的蛋白药物表达系统包括原核表达系统(如E. coli)、植物表达系统、真菌表达系统(如毕赤酵母、酿酒酵母)、昆虫表达系统(如SF9细胞)以及哺乳动物细胞表达系统(如中国仓鼠卵巢细胞和非洲绿猴肾细胞)。在这些系统中,尽管哺乳动物细胞表达系统广泛用于临床药物生产,但因其成本较高,E. coli表达系统因其高产量和低成本而成为最受欢迎的选择。
由于E. coli表达系统的培养简便、转化效率高、成本低且产量高,因此被广泛应用于各种蛋白的生产。例如,不需要糖基化修饰的人胰岛素和生长激素,及可在未糖基化情况下仍维持生物活性的蛋白如干扰素和白介素2等,都可以通过E. coli表达系统获得。
HCP的检测和鉴定方法中,ELISA和LC-MS方法为金标准。ELISA可高通量定量且成本低廉,而LC-MS则具备高定量与定性能力,但价格相对昂贵且通量较低。因此,两者的组合使用是实现HCP全面检测的重要策略。
研究表明,不同药物虽然采用相似的纯化工艺,或相同药物在不同的工艺条件下,其HCP残留的量差异显著,这也导致了国内外在药物HCP定量结果方面的差异。
E. coli HCP与CHO HCP之间存在明显的差异,可分为多种类型,例如:
1. 黏附素(如Curli,CsgA),形成淀粉样纤维,促进生物膜的形成;
2. 毒素(如α-溶血素),能够溶解红细胞和上皮细胞;
3. 侵袭素(如OmpA),促进E. coli侵袭血脑屏障,抵抗补体攻击;
4. 免疫逃逸相关蛋白(如LPS),诱导炎症反应但逃避免疫识别;
5. 分泌系统效应蛋白(如EspC),破坏上皮屏障;
6. 宿主互作效应蛋白(如NleH),通过抑制NF-κB通路减少炎症;
7. 噬菌体/质粒编码毒力蛋白(如Colibactin),诱导DNA损伤。
根据Jones等的研究,HCP的残留不仅可能具有免疫原性,还可能影响药物辅料的稳定性。因此,针对高风险宿主细胞的基因敲除或使用空载HCP模拟药物生产和纯化流程中的HCP残留分析变得尤为重要。在药物优化和纯化过程中,某些难以去除的HCP仍然是主要挑战。Zhu等的研究显示,E. coli表达的疟疾疫苗在纯化过程中的HCP含量范围大致在90 ng/mL至1100 ppm,而临床上能被接受的HCP含量范围仅为<100 ppm。
因此,对HCP的监测与调查至关重要,必须确保全面检测,以提升检测的灵敏度与覆盖度。
近期,不朽情缘MG推出的新型E. coli HCP(6S)ELISA/EH-E0022-3与美国Cygnus/F410产品进行了对比分析。从标定曲线范围、样本相对变化率、样本检测浓度及基线四个方面进行了评估,显示出以下优势:
1. 较低的基线,能够排除更多非特异性结合;
2. 稳定的样本相对变化率,检测区间广泛;
3. 更高的样本检测浓度。
最终,不朽情缘MG在生物制药行业内致力于提供专业的技术与服务,推动生命科学领域的持续创新,确保产品的核心竞争力并为人类健康做出积极贡献。
全国客户服务热线
17154030874
总部地址:乌鲁木齐南溪区谢街道70号